Если бы писателю-беллетристу пришлось заняться «биографией» цезия, то он, может быть, начал так: «Открыт цезий сравнительно недавно, в 1860 г., в минеральных водах известных целебных источников Шварцвальда (Баден-Баден и др.). За короткий исторический срок прошел блистательный путь — от редкого, никому не ведомого химического элемента до стратегического металла. Принадлежит к трудовой семье щелочных металлов, но в жилах его течет голубая кровь последнего в роде… Впрочем, это нисколько не мешает ему общаться с другими элементами и даже, если они не столь знамениты, он охотно вступает с ними в контакты и завязывает прочные связи.
Цезий
В настоящее время работает одновременно в нескольких отраслях: в электронике и автоматике, в радиолокации и кино, в атомных реакторах и на космических кораблях…». Не принимая всерьез шутливого тона и некоторых явно литературных преувеличений, это жизнеописание можно смело принять за «роман без вранья». Не беспредметен разговор о «голубой крови» цезия — впервые он был обнаружен по двум ярким линиям в синей области спектра и латинское слово «caesius», от которого произошло его название, означает небесно-голубой. Неоспоримо утверждение о том, что цезий практически последний в ряду щелочных металлов. Правда, еще Менделеев предусмотрительно оставил в своей таблице пустую клетку для «экацезия», который должен был следовать в I группе за цезием. И этот элемент (франций) в 1939 г. был открыт. Однако франций существует лишь в виде быстро распадающихся радиоактивных изотопов с периодами полураспада в несколько минут, секунд или даже тысячных долей секунды. Наконец, правда и то, что цезий применяется в некоторых важнейших областях современной техники и науки.
Общие сведения:
| 100 | Общие сведения | |
| 101 | Название | Цезий |
| 102 | Прежнее название | |
| 103 | Латинское название | Caesium |
| 104 | Английское название | Caesium, Cesium (в США) |
| 105 | Символ | Cs |
| 106 | Атомный номер (номер в таблице) | 55 |
| 107 | Тип | Металл |
| 108 | Группа | Щелочной металл |
| 109 | Открыт | Роберт Вильгельм Бунзен и Густав Роберт Кирхгоф, Германия, 1860 г. |
| 110 | Год открытия | 1860 г. |
| 111 | Внешний вид и пр. | Очень мягкий, вязкий серебристо-жёлтый металл |
| 112 | Происхождение | Природный материал |
| 113 | Модификации | |
| 114 | Аллотропные модификации | |
| 115 | Температура и иные условия перехода аллотропных модификаций друг в друга | |
| 116 | Конденсат Бозе-Эйнштейна | 33Cs |
| 117 | Двумерные материалы | |
| 118 | Содержание в атмосфере и воздухе (по массе) | 0 % |
| 119 | Содержание в земной коре (по массе) | 0,00019 % |
| 120 | Содержание в морях и океанах (по массе) | 5,0·10-8 % |
| 121 | Содержание во Вселенной и космосе (по массе) | 8,0·10-8 % |
| 122 | Содержание в Солнце (по массе) | 8,0·10-7 % |
| 123 | Содержание в метеоритах (по массе) | 0,000014 % |
| 124 | Содержание в организме человека (по массе) | 2,0·10-6 % |
Исторические предпосылки
Заслуга открытия электронной формулы цезия принадлежит химикам из Германии, выдающимся умам в свой области Кирхгоффу, Бунзену. Это событие случилось в далеком 1860 году. В тот период начали активно менять только-только изобретенную методику спектроскопии пламенем, и в ходе своих экспериментов немецкие ученые обнаружили прежде неизвестный общественности химический элемент – цезий. В тот момент цезий был представлен в качестве получателя, что актуально для фотоэлементов, электронных ламп.
Заметные изменения в истории определения и выделения элемента случились в 1967-м. С учетом сделанного Эйнштейном заявления о том, что скорость света можно считать наиболее постоянным фактором измерения, присущим нашей вселенной, было решено выделить цезий 133. Это стало важным моментом в расширении спектра применения химического элемента цезия – в частности, на нем изготавливают атомные часы.
Свойства атома цезия:
| 200 | Свойства атома | |
| 201 | Атомная масса (молярная масса) | 132,9054519(2) а.е.м. (г/моль) |
| 202 | Электронная конфигурация | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 6s1 |
| 203 | Электронная оболочка | K2 L8 M18 N18 O8 P1 Q0 R0 |
| 204 | Радиус атома (вычисленный) | 298 пм |
| 205 | Эмпирический радиус атома | 265 пм |
| 206 | Ковалентный радиус* | 244 пм |
| 207 | Радиус иона (кристаллический) | Cs+ 181 (6) пм, 188 (8) пм, 195 (10) пм, 202 (12) пм (в скобках указано координационное число – характеристика, которая определяет число ближайших частиц (ионов или атомов) в молекуле или кристалле) |
| 208 | Радиус Ван-дер-Ваальса | 343 пм |
| 209 | Электроны, Протоны, Нейтроны | 55 электронов, 55 протонов, 78 нейтронов |
| 210 | Семейство (блок) | элемент s-семейства |
| 211 | Период в периодической таблице | 6 |
| 212 | Группа в периодической таблице | 1-ая группа (по старой классификации – главная подгруппа 1-ой группы) |
| 213 | Эмиссионный спектр излучения |
Сочетаемость и особенности
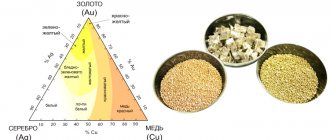
У цезия есть способность вступать в реакции с щелочными соединениями, металлами. Также элемент формирует оксиды цезия. Кроме того, наблюдаются реакции с ртутными смесями, золотом. Особенности взаимодействия с другими соединениями, а также температурные режимы, при которых реакции возможны, декларируют возможные межметаллические составы. В частности, цезий является исходным компонентом для формирования фоточувствительных соединений. Для этого проводят реакцию металла с участием тория, сурьмы, галлия, индия.
Кроме оксида цезия, интерес у химиков вызывают и результаты взаимодействия с рядом щелочных элементов. В то же время нужно учитывать, что металл не может реагировать с литием. Для каждого из сплавов цезия характерен собственный оттенок. Некоторые смеси – это черно-фиолетовые соединения, другие окрашены в золотой оттенок, а третьи практически бесцветны, но с ярко выраженным металлическим блеском.
Химические свойства цезия:
| 300 | Химические свойства | |
| 301 | Степени окисления | -1, +1 |
| 302 | Валентность | I |
| 303 | Электроотрицательность | 0,79 (шкала Полинга) |
| 304 | Энергия ионизации (первый электрон) | 375,7 кДж/моль (3,893905695(24) эВ) |
| 305 | Электродный потенциал | Cs+ + e— → Cs, Eo = -2,923 В |
| 306 | Энергия сродства атома к электрону | 45,505(3) кДж/моль (0,471630(25) эВ) |
Работа продолжается
Не секрет, что открытие элемента и получение его в чистом виде – это две совершенно разные задачи, хоть и связанные между собой. Когда стало ясно, что цезий встречается очень редко, ученые начали разрабатывать методики синтезирования металла в лабораторных условиях. Первое время казалось, что это совершенно непосильная задача, если применять доступные в те времена средства и технику. Бунзену за долгие годы так и не удалось выделить металлический цезий в чистом его виде. Лишь два десятилетия спустя передовые химики смогли наконец решить эту задачу.
Прорыв произошёл в 1882-м, когда Сеттерберг из Швеции провел электролиз смеси, на четыре части состоящей из цианидов цезия, к которым была примешана одна часть бария. Последний компонент использовался, чтобы сделать температуру плавления меньше. Цианиды, как в этот момент уже знали ученые, представляли собой очень опасные компоненты. В то же время за счет бария формировалось загрязнение, что не позволяло получить более-менее удовлетворительное количество цезия. Было ясно, что методика требует существенных доработок. Хорошее предложение в этой сфере было вынесено на обсуждение научного сообщества Бекетовым. Именно тогда внимание привлекла гидроокись цезия. Если восстановить это соединение, применяя металлический магний, повышая нагрев и используя водородный ток, можно добиться несколько лучшего результата, нежели доказанный шведским химиком. Впрочем, реальные эксперименты показали, что выход вдвое меньше, нежели рассчитываемый в теории.
Физические свойства цезия:
| 400 | Физические свойства | |
| 401 | Плотность* | 1,93 г/см3 (при 20 °C и иных стандартных условиях, состояние вещества – твердое тело), 1,887 г/см3 (при температуре плавления 28,5°C и иных стандартных условиях, состояние вещества – твердое тело), 1,843 г/см3 (при температуре плавления 28,5 °C и иных стандартных условиях, состояние вещества – жидкость), 1,78 г/см3 (при 127 °C и иных стандартных условиях, состояние вещества – жидкость), 1,552 г/см3 (при 527 °C и иных стандартных условиях, состояние вещества – жидкость) |
| 402 | Температура плавления | 28,5 °C (301,7 K, 83,3 °F) |
| 403 | Температура кипения* | 671 °C (944 K, 1240 °F) |
| 404 | Температура сублимации | |
| 405 | Температура разложения | |
| 406 | Температура самовоспламенения смеси газа с воздухом | |
| 407 | Удельная теплота плавления (энтальпия плавления ΔHпл) | 2,09 кДж/моль |
| 408 | Удельная теплота испарения (энтальпия кипения ΔHкип)* | 63,9 кДж/моль |
| 409 | Удельная теплоемкость при постоянном давлении | |
| 410 | Молярная теплоёмкость | 32,21 Дж/(K·моль) |
| 411 | Молярный объём | 70,732 см³/моль |
| 412 | Теплопроводность | 35,9 Вт/(м·К) (при стандартных условиях), 35,9 Вт/(м·К) (при 300 K) |
| 413 | Коэффициент теплового расширения | |
| 414 | Коэффициент температуропроводности | |
| 415 | Критическая температура* | |
| 416 | Критическое давление | |
| 417 | Критическая плотность | |
| 418 | Тройная точка | |
| 419 | Давление паров (мм.рт.ст.) | |
| 420 | Давление паров (Па) | |
| 421 | Стандартная энтальпия образования ΔH | |
| 422 | Стандартная энергия Гиббса образования ΔG | |
| 423 | Стандартная энтропия вещества S | |
| 424 | Стандартная мольная теплоемкость Cp | |
| 425 | Энтальпия диссоциации ΔHдисс | |
| 426 | Диэлектрическая проницаемость | |
| 427 | Магнитный тип | |
| 428 | Точка Кюри | |
| 429 | Объемная магнитная восприимчивость | |
| 430 | Удельная магнитная восприимчивость | |
| 431 | Молярная магнитная восприимчивость | |
| 432 | Электрический тип | |
| 433 | Электропроводность в твердой фазе | |
| 434 | Удельное электрическое сопротивление | |
| 435 | Сверхпроводимость при температуре | |
| 436 | Критическое магнитное поле разрушения сверхпроводимости | |
| 437 | Запрещенная зона | |
| 438 | Концентрация носителей заряда | |
| 439 | Твёрдость по Моосу | |
| 440 | Твёрдость по Бринеллю | |
| 441 | Твёрдость по Виккерсу | |
| 442 | Скорость звука | |
| 443 | Поверхностное натяжение | |
| 444 | Динамическая вязкость газов и жидкостей | |
| 445 | Взрывоопасные концентрации смеси газа с воздухом, % объёмных | |
| 446 | Взрывоопасные концентрации смеси газа с кислородом, % объёмных | |
| 446 | Предел прочности на растяжение | |
| 447 | Предел текучести | |
| 448 | Предел удлинения | |
| 449 | Модуль Юнга | |
| 450 | Модуль сдвига | |
| 451 | Объемный модуль упругости | |
| 452 | Коэффициент Пуассона | |
| 453 | Коэффициент преломления |
Такой похожий, но совсем другой
При сравнении отличительных особенностей цезия и рубидия, а также других элементов, встречающихся крайне редко, удалось выявить, что цезию свойственно формирование уникальных минералов, на что не способны прочие соединения. Именно таким образом получаются поллуцит, родицит, авогадрит.
Родицит, как выяснили ученые, встречается в исключительно редко. Аналогичным образом очень сложно найти авогадрит. Поллуцит несколько более распространен, в ряде случаев обнаруживались небольшие залежи. Они обладают очень низкой мощностью, но содержат цезий в количестве 20-35 процентов от общей массы. Самые важные, с точки зрения общественности, поллуциты были обнаружены в американских недрах и на территории России. Также есть шведские разработки, казахстанские. Известно, что поллуцит найден на юго-западе Африканского континента.
Кристаллическая решётка цезия:
| 500 | Кристаллическая решётка | |
| 511 | Кристаллическая решётка #1 | |
| 512 | Структура решётки | Кубическая объёмно-центрированная |
| 513 | Параметры решётки | 6,140 Å |
| 514 | Отношение c/a | |
| 515 | Температура Дебая | 39,2 K |
| 516 | Название пространственной группы симметрии | Im_ 3m |
| 517 | Номер пространственной группы симметрии | 229 |
Активность и реакции
В ходе многочисленных исследований ученые смогли определить, что цезию присуща удивительная активность, в норме не свойственная металлам. При контакте с воздухом происходит возгорание, которое приводит к выделению надпероксида. Добиться окиси можно, если ограничить доступ кислорода к реагентам. Есть возможность формирования субоксидов.
Если цезий контактирует с фосфором, серой, галогеном, это провоцирует сопровождающуюся взрывом реакцию. Также взрыв сопутствует реакции с водой. Используя кристаллизатор, стакан, можно столкнуться с тем, что емкость буквально разлетается на кусочки. Также возможна реакция со льдом, если температура по шкале Цельсия – не ниже 116 градусов. В результате такой реакции продуцируются водород, гидроксид.
Висмут
Обычно это выглядит так:
nexmetal.com
Но при правильных условиях это может выглядеть так:
Wikipedia
Мы рекомендуем воспользоваться поиском картинок на Яндексе или в Google по запросу «Кристаллы висмута», чтобы увидеть все чудеса, которые может произвести висмут.
Некоторые другие интересные факты о висмуте:
- Висмут (висмут-209, самый распространенный изотоп) радиоактивен, но имеет один из самых длинных периодов полураспада из когда-либо измеренных. Его период полураспада составляет 1,9×10 ^ 19 лет, или примерно в миллиард раз дольше, чем существует Вселенная.
- Висмут — самый сильный природный диамагнитный металл из известных. Диамагнитные материалы при воздействии магнитного поля создают в ответ отталкивающее поле. Итак, с некоторыми сильными магнитами вы можете заставить висмут подниматься.
- Висмут обладает необычайно низкой токсичностью для тяжелых металлов. Его соседи по периодической диаграмме – полоний, сурьма и свинец – довольно токсичны, но висмут относительно безвреден. Из-за этого висмут исследуется как альтернатива свинцу для некоторых применений.
- Большинство людей употребляют висмут в своей жизни. Активным ингредиентом пепто-висмола является субсалицилат висмута.
Применение
В 1962 г. из США началась поставка раздражающего вещества CS в Южный Вьетнам. Через 2 года данное соединение было применено в борьбе с партизанским движением во время гражданской войны. С этого момента оно начало широко использоваться американскими войсками. По некоторым данным, общее количество израсходованного хлорбензальмалонодинитрила за годы вьетнамской войны составляет более 6 000 тонн.
После успешного применения в военных целях его начали использовать в полиции при наведении общественного порядка. Однако, когда были обнаружены его тератогенные свойства, оно было снято с вооружения в европейских странах. Согласно Конвенции 1993 г. о химическом оружии это соединение запрещено применять в военных целях, но в ряде стран (Бахрейн, Непал, Южная Корея, Египет) оно все еще в ходу.
Существуют более безопасные ирританты, по своему действию сходные с веществом CS. Морфолид пеларгоновой кислоты в виде аэрозоля также раздражает органы зрения и дыхания, но эти симптомы проходят быстрее (за 10-15 минут на свежем воздухе) и не требуют лечения. Данный химикат обладает гораздо меньшей токсичностью.
История создания
Вещество CS впервые было получено в 1928 году в Миддлбери-колледже в Вермонте (Англия). Его синтезировали двое американских ученых-химиков Б. Корсон и Р. Стоун. Они занимались систематическим изучением реакций альдегидов и кетонов с динитрилом малоновой кислоты. В результате были получены несколько новых соединений, среди которых было и хлорбензальмалонодинитрил. Название вещества CS произошло от первых букв фамилий его первооткрывателей (Corson и Stoughton). Уже тогда были замечены его психофизиологические свойства. В своем отчете на 13 страницах ученые зафиксировали, что оно вызывает сильное слезотечение и чихание.
В то время данное соединение не привлекло к себе большого внимания. Однако в конце 50-х гг. XX в. им заинтересовались специалисты Министерства обороны Великобритании, которые в то время активно занимались поиском эффективного химического оружия. Вскоре оно было испытано на практике сначала на животных, затем на добровольцах английской армии, а после этого – во время проведения боевых действий в некоторых странах. На химическом заводе в Нэнскъюке был налажен его промышленный синтез, а в 1954 г. отравляющее вещество CS было принято на вооружение полицией и национальной гвардией США.
Изотопы
Основная статья: Изотопы цезия
Известны изотопы цезия с массовыми числами от 112 до 151 (количество протонов 55, нейтронов от 57 до 96), и 22 ядерных изомеров. Природный цезий — моноизотопный элемент, состоящий из единственного стабильного изотопа 133Cs.
Схема распада Cs-137
Самым долгоживущим искусственным радиоактивным нуклидом цезия является 135Cs с периодом полураспада T
1/2 около 2,3 миллиона лет. Другой относительно долгоживущий изотоп 137Cs (
T
1/2 = 30,17 года).
Цезий-137 является одним из виновников радиоактивного загрязнения биосферы, так как образуется при делении ядер в ядерных реакторах и при испытаниях ядерного оружия. Цезий-137 претерпевает бета-распад, дочерний изотоп стабильный барий-137.
Применять с умом
Не только цезий, но и известные на основе этого металла соединения используются в настоящее время очень широко. Без них невозможно представить себе конструирование радиотехники, незаменимы они и в электронике. Активно применяется соединение и вариации цезия в химии, промышленности, офтальмологической сфере, медицинской. Не обойден вниманием цезий и в рамках развития применимых в космосе технологий, а также ядерной энергетики.
В настоящее время распространено использовать цезий при конструировании фотоэлементов. Бромид, иодид этого металла необходимы для создания систем инфракрасного видения. Полученные промышленным путем монокристаллы допускается использовать в качестве элементов детекторов, позволяющих фиксировать ионизирующее излучение. Некоторые соединения на основе цезия активно используются как катализаторы в процессах промышленности. Это необходимо при создании аммиака, формировании окиси этилена и продуцировании бутадиена.
Влияние на организм человека
Хлорбензальмалонодинитрил в виде аэрозоля может вызвать следующие негативные явления:
- сильное слезотечение;
- чувство жжения в носоглотке;
- боль за грудиной;
- конъюнктивит;
- сухость, раздражение кожи;
- носовое кровотечение.
Хотя вещество CS не относится к смертельно опасным, оно может вызвать повреждение легких, печени и сердца при концентрации от 0,27 мг/л и выше, особенно в замкнутых пространствах и при длительном воздействии. Опыты на животных показали также, что оно обладает тератогенным эффектом. Опасной концентрацией в воздухе является 0,002 мг/л. Токсическое действие обнаруживается в течение нескольких секунд, а проходит за 15-30 минут. Покраснение кожи может сохраняться в течение нескольких часов.
Получение
При промышленном получении цезий в виде соединений извлекается из минерала поллуцита. Это делается хлоридным или сульфатным вскрытием. Первое включает обработку исходного минерала подогретой соляной кислотой, добавление хлорида сурьмы SbCl3 для осаждения соединения Cs3[Sb2Cl9] и промывку горячей водой или раствором аммиака с образованием хлорида цезия CsCl. При втором — минерал обрабатывается подогретой серной кислотой с образованием алюмоцезиевых квасцов CsAl(SO4)2·12H2O.
Для получения цезия достаточной степени чистоты требуется многократная ректификация в вакууме, очистка от механических примесей на металлокерамических фильтрах, нагревание с геттерами для удаления следов водорода, азота, кислорода и многократная ступенчатая кристаллизация.
Сложности получения цезия обусловливают постоянный поиск его минералов: извлечение этого металла из руд неполное, в процессе эксплуатации материала он рассеивается и потому безвозвратно теряется, Промышленность нуждается именно в очень чистом материале (на уровне 99,9—99,999 %), и это является одной из труднейших задач в металлургии редких элементов.
В России переработка и извлечение солей цезия из поллуцита ведется в Новосибирске на ЗАО «Завод редких металлов».
Существует несколько лабораторных методов получения цезия. Он может быть получен:
- нагревом в вакууме смеси хромата или дихромата цезия с цирконием;
- разложением азида цезия в вакууме;
- нагревом смеси хлорида цезия и специально подготовленного кальция.
Все методы являются трудоёмкими. Второй позволяет получить высокочистый металл, однако является взрывоопасным и требует на реализацию несколько суток.
Формы
Для получения аэрозоля хлорбензальмалонодинитрила применяется несколько способов:
- растворение в органических растворителях;
- расплавление и распыление в жидкой форме;
- использование силиконизированного порошка (для предотвращения комкования активного вещества);
- введение в состав боеприпасов взрывного действия (артиллерийские снаряды, химические бомбы, авиационные кассеты, ручные гранаты), пиротехнических смесей;
- применение в механических генераторах аэрозолей и диспергаторах.
Гидроксид: особенности
В ходе изучения продуктов реакции, производимых цезием, химики выявили, что получаемый гидроксид – это очень сильное основание. Взаимодействуя с ним, необходимо помнить, что при высокой концентрации это соединение запросто может разрушить стекло даже без дополнительного нагрева. А вот при повышении температуры гидроксид без труда плавит никель, железо, кобальт. Аналогичным будет влияние на циркониевый диоксид, корунд, платину. Если в реакции принимает участие кислород, гидроксид цезия крайне быстро разрушает серебро, золото. Если ограничить поступление кислорода, процесс протекает относительно медленно, но все же не останавливается. Стойкостью к гидроксиду цезия обладают родий и несколько сплавов этого соединения.
Франций
Франций ОЧЕНЬ реактивный и имеет атомный номер 87.
Франций очень реакционноспособный и радиоактивный элемент. Поскольку периодего полураспада составляет 22 минуты, он очень реактивный.
Фактически это никогда не проверялось из-за рисков, которые это несет. Тем не менее ученые сделали копию того, на что это было бы похоже, если бы вы уронили его в воду.
Посмотрите, к чему это привело бы:
Вот некоторые фотографии, на которых тестировался франций (но только с небольшим количеством)
Наконец, вот так выглядит франций.